Какой воздух при одинаковом объеме и одинаковом давлении
Содержание статьи
Какой воздух при одинаковом объеме и одинаковом давлении
Какой воздух тяжелее: сухой или влажный?
Ответ на данный вопрос не так прост, как кажется. Большинство людей ответит, что тяжелее влажный воздух, так как там содержатся пары воды, и они окажутся неправы.
Разбор данного вопроса стоит начать с изучения состава нашей атмосферы.
Как видно из диаграммы, наша атмосфера в основном состоит из молекулярных азота и кислорода — N2 и O2 соответственно. Их молекулярные массы составляют 28 грамм/моль и 32 грамм/моль, исходя из таблицы Менделеева.
Все рассуждения будут основаны на одном законе, который вывел человек, некогда живший в Италии — Амедео Авогадро.
Закон Авогадро говорит о следующем: число молекул всегда одно и то же в одинаковых объемах любых газов, но важно, чтобы условия (температура, давление и прочее), в которых будут проводиться измерения, были одинаковы для всех газов.
Проведем мысленный эксперимент: возьмем один кубометр абсолютно сухого воздуха, и будем его понемногу увлажнять таким образом, чтобы не менялись условия проведения эксперимента. Сделать это можно только заменяя молекулы воздуха молекулами воды.
Химическая формула воды ни для кого не секрет — H2O и молекулярная масса составляет 18 г/моль.
Таким образом, мы взамен более тяжелых молекул азота (28 г/моль) и кислорода (32г/моль) помещаем более легкие молекулы воды (18 г/моль), и общая масса газовой смеси уменьшается.
И так, мы доказали, что сухой воздух окажется тяжелее, чем влажный. Но более важным выводом является то, что плотность влажного воздуха ниже, чем сухого, и как следствие движение через него более легкое.
Так если при игре в бейсбол к мячу приложить одинаковое количество энергии, то он полетит дальше во влажном воздухе.
Это стало проблемой в США, когда во время игры в крытых стадионах домашняя команда включала систему кондиционирования, чтобы сделать воздух более сухим. Таким образом воздух становился плотнее, и команда противников отбивала мячи на менее длинные дистанции.
Надеюсь, что для вас эта статья была интересной и познавательной. Если она вам понравилась, то не забывайте ее оценить и подписаться на канал, чтобы читать больше интересного из мира науки. Всего вам доброго, и до скорых встреч! ????
Источник
Почему горячий воздух легче холодного
Нас окружает большое количество явлений, к которым мы давно привыкли. Причём настолько, что нередко не задаёмся вопросами, почему так, а не иначе, или что это означает. Например, всё знают, что тёплый воздух легче холодного и от этого поднимается вверх. Но что означает «легче»?
То есть простой вроде бы вопрос на самом деле таковым не является. И даже вызывает горячие споры .
Дело в объёме, а не в массе
На самом деле, конечно, говорить о том, что горячий воздух «легче» холодного, несколько некорректно. Дело в том, что по мере повышения температуры газа скорость молекул нарастает. Следовательно, расстояние между ними будет тоже увеличиваться. А это означает, что горячий воздух станет занимать больше пространства.
Таким образом, один и тот же объём газа в нагретом состоянии станет меньше давить на квадратный сантиметр или любую другую единицу поверхности. Этим и объясняется его «лёгкость». Но за счёт чего такое стало возможным?
От температуры зависит плотность газа. Наверх постоянно будет стремиться тот, у которого плотность меньше. Или, если перефразировать, у кого при равной массе больше объём. Это касается всех тел и распространяется и на газы тоже.
Молярно-кинетическая теория газов
Вопрос с лёгким горячим воздухом хорошо объясняется этой теорией. Среднюю кинетическую энергию молекул определяет температура. Зависимость простая: чем выше температура, тем выше кинетическая энергия молекул газа. А это означает, что молекулы начинают двигаться быстрее. И в результате данного процесса расстояние между ними возрастает. За счёт этого плотность газа и уменьшается, поскольку увеличивается объём.
Однако земная гравитация мешает молекулам газа в процессе разогрева отправляться в путешествие в космос. То есть на воздух действует несколько сил. И в то время как одни «выталкивают» его при нагревании на поверхность, другие притягивают вниз.
Так ли всё очевидно?
Кажется, что для понимания процессов, которые происходят с тёплым и холодным воздухом, достаточно школьного курса знаний. Однако если начать разбираться в происходящем глубже, то возникает немало интересных вопросов. Например, выше говорилось о кинетической энергии у молекул. Но откуда она у них вообще берётся?
Движение молекул связано с энергией импульса, которая заставляет их стремиться за снарядами. Например, если посмотреть на пар, то на него воздействует краснофотонное излучение. Оно импульсами и задаёт движение. В итоге разреженный газ начинает стремиться в область, где давление не такое высокое, как внизу, а плотность меньше. И это движение будет сохраняться до тех пор, пока поток воздуха не встретит преграду или пока он не остынет.
Почему тёплый воздух движется наверх?
Воздух нагревается, расширяется, после чего устремляется наверх. В физике это носит название конвективных перемещений. В реальной жизни на движение воздушных масс влияет не один фактор, а целый ряд. В частности, это разница температур, показателей давления и гравитационная сила.
Допустим, если вы откроете форточку зимой, то оттуда к нам начнёт попадать холодный воздух. Его температура заметно ниже температуры тех масс, которые находятся в помещении. Так что зимой разницу между потоками воздуха можно даже наблюдать: холодный воздух буквально стелется по полу.
Молекулы воздуха обладают излучением. Оно возрастает по мере увеличения температур. В процессе активности молекулы как бы отстреливают импульсы, причём благоприятные условия для такой активности создаются в области сниженного давления. То есть наверху.
В итоге тёплые молекулы воздуха движутся наверх. А их место занимают более холодные. То есть благодаря гравитации холодный воздух будет опускаться вниз. Именно так и работает конвекция .
Зачем эти знания нужны на практике?
Понимание конвекции позволяет создавать системы отопления. Разобраться с микроклиматом в доме без подобных знаний в противном случае бы не получилось. Главное — вспомнить физику.
Источник
Какой воздух при одинаковом объеме и одинаковом давлении
Владельцы сайта
Урок №40. Закон Авогадро. Молярный объем газов
Закон Авогадро: в равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул. (1811 г, итальянский учёный Амедео Авогадро)
Одинаковое число молекул различных газов при одинаковых условиях занимает одинаковый объём.
Так, 6,02 ∙ 10 23 молекул (1 моль) любого газа и любой смеси газов при (н.у.) занимает объём равный 22,4 л .
Такой объём называется молярным объёмом и обозначается Vm
Молярный объём — это постоянная величина для веществ — газов при нормальных условиях (н.у.):
Взаимосвязь молярной массы, молярного объёма, числа Авогадро и количества вещества:
Образец: Какой объем занимает 0,2 моль N 2 при н.у.?
= 0,2 моль · 22,4 л / моль = 4,48 л
Ответ: V (N2 ) = 4,48 л
Задачи для самостоятельного решения
Решите задачи по приведённому образцу:
1. Какой объем занимают 5 моль О2 при н.у.?
2. Какой объем занимают 2,5 моль Н2 при н.у.?
Образец: Какое количество вещества содержит водород объемом 33,6 л при н.у.?
Ответ: ν (Н2) = 1,5 моль
Задачи для самостоятельного решения
Решите задачи по приведённому образцу:
1. Какое количество вещества содержит кислород объемом 0,224 л при н.у.?
2. Какое количество вещества содержит углекислый газ объемом 4,48 л при н.у.?
Образец: Какой объем займут 56 г. газа СО при н.у.?
ν (CO) = V(CO) / Vm , следовательно
Неизвестное количество вещества найдём по формуле:
M(CO) = Ar(C) + Ar(O) = 12 + 16 = 28 г/моль
ν (СО) = m/M = 56 г / 28 г/моль = 2 моль
V (CO ) = ν (CO) · Vm = 2 моль · 22,4 л/моль
Ответ: V (CO ) = 44,8 л
Задачи для самостоятельного решения
Решите задачи по приведённому образцу:
Образец: В каком объеме содержится 3·10 23 молекул водорода Н2 при н.у.?
Na = 6,02 ·10 23 моль -1
Неизвестное количество вещества найдём по формуле:
ν = N / Na = 3·10 23 / 6,02 ·10 23 моль -1 = 0,48 моль
Задачи для самостоятельного решения
Решите задачи по приведённому образцу:
1. В каком объеме содержится 12,04 ·10 23 молекул углекислого газа — СО2 при н.у.?
2. В каком объеме содержится 3,01·10 23 молекул кислорода — О2 при н.у.?
Источник
Источник
Сухой и влажный воздух при одинаковых давлениях и температурах
Какой воздух тяжелее: сухой или влажный?
Ответ на данный вопрос не так прост, как кажется. Большинство людей ответит, что тяжелее влажный воздух, так как там содержатся пары воды, и они окажутся неправы.
Разбор данного вопроса стоит начать с изучения состава нашей атмосферы.
Как видно из диаграммы, наша атмосфера в основном состоит из молекулярных азота и кислорода — N2 и O2 соответственно. Их молекулярные массы составляют 28 грамм/моль и 32 грамм/моль, исходя из таблицы Менделеева.
Все рассуждения будут основаны на одном законе, который вывел человек, некогда живший в Италии — Амедео Авогадро.
Закон Авогадро говорит о следующем: число молекул всегда одно и то же в одинаковых объемах любых газов, но важно, чтобы условия (температура, давление и прочее), в которых будут проводиться измерения, были одинаковы для всех газов.
Проведем мысленный эксперимент: возьмем один кубометр абсолютно сухого воздуха, и будем его понемногу увлажнять таким образом, чтобы не менялись условия проведения эксперимента. Сделать это можно только заменяя молекулы воздуха молекулами воды.
Химическая формула воды ни для кого не секрет — H2O и молекулярная масса составляет 18 г/моль.
Таким образом, мы взамен более тяжелых молекул азота (28 г/моль) и кислорода (32г/моль) помещаем более легкие молекулы воды (18 г/моль), и общая масса газовой смеси уменьшается.
И так, мы доказали, что сухой воздух окажется тяжелее, чем влажный. Но более важным выводом является то, что плотность влажного воздуха ниже, чем сухого, и как следствие движение через него более легкое.
Так если при игре в бейсбол к мячу приложить одинаковое количество энергии, то он полетит дальше во влажном воздухе.
Это стало проблемой в США, когда во время игры в крытых стадионах домашняя команда включала систему кондиционирования, чтобы сделать воздух более сухим. Таким образом воздух становился плотнее, и команда противников отбивала мячи на менее длинные дистанции.
Надеюсь, что для вас эта статья была интересной и познавательной. Если она вам понравилась, то не забывайте ее оценить и подписаться на канал, чтобы читать больше интересного из мира науки. Всего вам доброго, и до скорых встреч! ????
Источник
Почему влажный воздух легче сухого?
Сухой воздух действительно тяжелее, чем влажный. Хотя многие скажут, что это не так, ведь в сухом воздухе не содержатся молекулы воды. Однако, нужно вспомнить закон Авогадро, согласно которому: «равные объёмы любых газов при одинаковых условиях содержат равное число молекул». Поэтому, если мы возьмем одинаковые объемы сухого и влажного воздуха, то в сухом воздухе хоть и не будет воды, но будут содержаться такие газы как — азот, аргон, кислород. И если мы заменим одну из этих молекул на воду (помним, что количество молекул изначально равное!), то их общая масса станет меньше. И мы можем сделать вывод, что сухой воздух тяжелее чем влажный.
Вода при замерзании расширяется или сжимается?
У воды парадоксальные свойства. Теплая вода при охлаждении уменьшается в объеме до тех пор, пока ее температура не понизится приблизительно до 4°С. При этой температуре вода достигает максимальной плотности и наименьшего объема. Но если воду охлаждать дальше ниже 4°С она начинает расширяться, пока температура не понизится до тройной точки (О °С). После этого жидкая вода начинает отвердевать и продолжает расширяться.
3 5 · Хороший ответ
Есть ли смысл в увлажнителях воздуха?
У меня в квартире влажность 20% хоть с открытым окном, хоть с помытым полом. Ну 22% максимум. Как итог — сухая кожа в цыпках и вечно заложенный нос. С этой напастью у меня борются (или борятся. ) два увлажнителя: механический Бонэко, который позиционируется как мойка воздуха, но на самом деле он увлажнитель, и ультразвуковой Филлипс. Бонэко нравится больше, но он будит по ночам громким бульканьем из-за конструкции бачка с водой, к тому же они оба с вентилятором, из-за шума которых некомфортно спать. Сейчас рассматриваю вариант с паровым увлажнителем, мне кажется он потише.
Смысл определенно есть, но они стоят дорого, поэтому к покупке надо подойти основательно, т.к. многие аппараты просто дорогие игрушки с низкой производительностью и крохотным бачком для воды.
Источник
Почему влажный воздух легче?
Рассмотрим следующий пример. Конечно, хочется сказать, что влажный воздух тяжелее, поскольку в отличие от сухого в нем содержатся еще и молекулы воды. Однако если речь идет об одинаковых температуре и давлении, то закон Дальтона говорит: что если в сухой воздух добавить пары воды, то его давление возрастет. Чтобы давление влажного воздуха равнялось давлению сухого, необходимо во влажном воздухе уменьшить число молекул собственно воздуха, и ответ на вопрос о сравнении масс сухого и влажного воздуха не является таким уж примитивным.
Поэтому давайте аккуратно с помощью законов Клапейрона-Менделеева и Дальтона сравним массы сухого и влажного воздуха. Давление сухого воздуха, занимающего объем V определяется законом Клапейрона-Менделеева
где N — число молекул воздуха; T — его температура. Давление влажного воздуха в том же объеме при той же температуре определяется законом Дальтона
где N — число молекул воздуха; T — воды. Из сравнения формул (1) и (2) видим, что при одинаковых давлении, объеме и температуре сухой и влажный воздух содержат одинаковое число молекул. Поэтому сравнение масс сухого и влажного воздуха определяется сравнением массы одной молекулы воздуха и одной молекулы воды. Конечно, такого объекта как «молекула воздуха» в общем-то не существует, так как воздух — это смесь различных газов, в наибольшем количестве в которой представлены азот, кислород, аргон и углекислый газ. Тем не менее, понятие средней молярной массы воздуха можно ввести, и эта средняя молярная масса равна 29 г/моль. Поэтому можно считать, что масса одной «усредненной» молекулы воздуха равна 29 а.е.м. Масса одной молекулы воды равна 18 а.е.м. Из этих чисел следует, что влажный воздух легче сухого при одинаковых температурах и давлениях.
Немного о влажности воздуха
На Земле много открытых водоемов, с поверхности которых испаряется вода: океаны и моря занимают около 80 % поверхности Земли. Поэтому в воздухе всегда есть водяной пар.
Он легче воздуха, потому что молярная масса воды (18 * 10 -3 кг моль -1 ) меньше молярной массы азота и кислорода, из которых в основном состоит воздух. Поэтому водяной пар поднимается вверх. При этом он расширяется, так как в верхних слоях атмосферы давление ниже, чем у поверхности Земли. Этот процесс приближенно можно считать адиабатическим, потому что за то время, пока он происходит, теплообмен пара с окружающим воздухом не успевает произойти.
Как мы увидим далее, при охлаждении до некоторой температуры, которую называют точкой росы, водяной пар начинает конденсироваться, собираясь в крошечные капельки воды. Так образуются облака.
Они не падают потому, что парят в восходящих потоках воздуха подобно тому как парят дельтапланы. Но когда капли в облаках становятся слишком большими, они начинают все-таки падать: идет дождь.
Содержание водяного пара в воздухе часто характеризуют давлением, которое он оказывал бы, если бы не было других газов. Его называют парциальным давлением водяного пара. («Парциальный» в переводе с латинского означает «частичный».)
Мы чувствуем себя комфортно, когда давление водяного пара при комнатной температуре (20 ºС) составляет около 1,2 кПа.
Относительной влажностью воздуха φ называют выраженное в процентах отношение парциального давления p водяного пара к давлению pн насыщенного пара при той же температуре:
Комфортные условия для человека соответствуют относительной влажности 50-60 %. Если относительная влажность существенно меньше, воздух кажется нам сухим, а если больше — влажным. Когда относительная влажность приближается к 100 %, воздух воспринимается как сырой. Лужи при этом не высыхают, потому что процессы испарения воды и конденсации пара компенсируют друг друга.
Для человека величина влажности является очень важным параметром окружающей среды, т. к. наш организм очень активно реагирует на ее изменения. Например, такой механизм регуляции функционирования организма, как потоотделение, напрямую связан с температурой и влажностью окружающей среды. При высокой влажности процессы испарения влаги с поверхности кожи практически компенсируются процессами ее конденсации и нарушается отвод тепла от организма, что приводит к нарушениям терморегуляции. При низкой влажности процессы испарения влаги превалируют над процессами конденсации и организм теряет слишком много жидкости, что может привести к обезвоживанию.
Величина влажности важна не только для человека и других живых организмов, но и для протекания технологических процессов. Например, из-за известного свойства воды проводить электрический ток ее содержание в воздухе может серьезно влиять на корректную работу большинства электроприборов.
Кроме того, понятие влажности является важнейшим критерием оценивания погодных условий, что всем известно из прогнозов погоды. Стоит отметить, что если сравнивать влажность в различные времена года в привычных для нас климатических условиях, то она выше летом и ниже зимой, что связано, в частности, с интенсивностью процессов испарения при различных температурах.
Итак, об относительной влажности воздуха судят по тому, насколько водяной пар в воздухе близок к насыщению.
Если воздух с находящимся в нем ненасыщенным водяным паром изотермически сжимать, будет увеличиваться как давление воздуха, так и давление ненасыщенного пара. Но давление водяного пара будет увеличиваться только до тех пор, пока он не станет насыщенным!
При дальнейшем уменьшении объема давление воздуха будет продолжать увеличиваться, а давление водяного пара будет постоянным — оно будет оставаться равным давлению насыщенного пара при заданной температуре. Избыток пара сконденсируется, то есть превратится в воду.
Видео
Источник
Источник
1. Какой воздух легче холодный или теплый?
Бессмысленно продолжать делать то же самое и ждать других результатов (Эйнштейн)
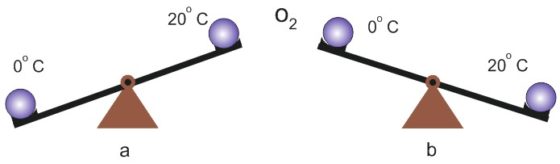
Рис. 1. Условно показана молекула кислорода на рычажных весах (детские качели) при разных температурах окружающей атмосферы. a — из наблюдений; b — по Эйнштейну.
Зададимся вопросом в стиле Якова Перельмана: какой воздух тяжелее холодный или теплый? После этого посмотрим ответы на форуме в интернете (ответы обозначены цифрами): 1) теплый; 2) холодный;3) холодный конечно; 4) тёплый воздух поднимается вверх, он легче; 5) холодный, поэтому он внизу всегда; 6) конечно теплый!; 7) тяжелей холодный, он опускается вниз, а теплый поднимается, значит легче; 8) тяжелее влажный воздух!; 9) холодный, вспомни, когда зимой открываешь форточку; 10) это и в садике знают, что тёплый легче, поэтому вверх стремится.
На тяжесть холодного воздуха ставок гораздо больше.
Мы народ северный и нас на таком вопросе не проведешь, открывая зимой форточку, наблюдаем, как холодный воздух буквально врывается в комнату, падает вниз к нашим ногам и расстилается по полу комнаты. А может он хочет нам поклониться за широкое гостеприимство? Не знаю, но это подтверждается визуально, когда холодный воздух, увлекая частицы пара, превращает их в видимый шлейф при конденсации. После чего выносится вердикт: холодный воздух тяжелее теплого, поэтому он устремляется вниз. Очередная зима, подкрепляет наши наблюдения и укрепляет правоту сказанного. Объясняем мы это плотностью — холодный воздух более плотный, теплый более разреженный.
Иногда для объяснения притягивают влажность воздуха. Поскольку, в зимний период на улице влаги больше, то влажный воздух должен весить якобы больше. Воздух — это смесь газов, состоящая на три четверти из азота и почти на четверть из кислорода и некоторого количества водяного пара. Количество остальных газов пренебрежимо мало, их не учитываем. Средняя молекулярная масса воздуха 29, молекулярная масса водяного пара 18. Об этом говорит и, упомянутый выше, Я. Перельман: «При одинаковом давлении и температуре кубометр влажного воздуха не тяжелее, а легче, чем кубометр сухого воздуха» [1].
Для выяснения сути данного явления в бытовых условиях можно пойти в баню, и пока не вспотели, понаблюдать за движением пара. Кто в баню не ходит пусть поставит эксперимент на своей кухне и нагреет кастрюлю с водой. Как только кастрюля закипит, пар с завихрениями устремится вверх, под купол вытяжной вентиляции. В бане этот процесс выражен еще более контрастно, первый ковш воды, брошенный на раскаленные камни, выбрасывает вверх белый шлейф пара. Мы видим восходящий паровой поток, который буквально вонзается в потолок, растекается по нему, стараясь его приподнять, и, постепенно охлаждаясь, начинает оседать, а затем конденсироваться на холодных металлических трубах.
По сравнению с окружающим воздухом пар перегрет, поэтому его молекулы более энергонасыщены.
Можно ли доверять нашим органолептическим органам? Для начала необходимо разобраться, почему холодный воздух уплотняется?
2. Почему плотность холодного воздуха больше чем теплого?
На самом ли деле теплый воздух легче холодного. Давайте проверим это утверждение и взвесим две молекулы кислорода теплую, при температуре +20º С и холодную, при температуре 0º С. Но как это сделать, на каких весах измерить разницу веса между молекулами? Судя по рисунку, автору удалось это сделать с помощью рычажных весов (детской качели).
Трудность заключается еще и в том, что мы не сможем в земных условиях точно оценить вес даже, заключенных в оболочку, достаточно больших одинаковых объемов воздуха. Оценке мешает эффект плавучести (статья «Гравитационная температура»). Остается одно, разобраться с этим явлением с энергетической точки зрения. Если мы возьмем молекулы одного и того же газа, но при разных температурах, то понятно, что молекула, имеющая более высокую температуру, будет более энергонасыщена и будет иметь более высокую скорость перемещения.
А за счет какой энергии вообще молекулы перемещаются? Классическая молекулярно-кинетическая теория на этот вопрос не дает вразумительного ответа. Этот физический процесс был основательно исследован в главе «Броуновское движение». Молекулы двигаются благодаря энергии импульсов придачи «вперед за снарядом». Под действием этих импульсов электромагнитного крафонного (краснофотонного) излучения, молекулы пара стремительно разлетаются в разные стороны, но в большей степени вверх (область пониженного давления), тем самым, разреживая и освобождая пространство, в которое устремляется новые молекулы. Те, в свою очередь, поступают как первые. Тем самым мы видим восходящий поток пара. Этот процесс в динамике идет по нормали до первой преграды — потолка.
Попутно еще один вопрос: за счет чего уплотняется холодный воздух?
Конвективные перемещения осуществляются за счет разности давлений, разности температур и гравитации. Холодный воздух из открытой форточки непрерывным потоком падает на пол нашей комнаты. Да, температура холодного воздуха ниже, чем теплого и что из этого следует? Ранее было выяснено, что гравитация квантуется, т.е. передается импульсами. Количество этих импульсов гравитационного излучения земли и нашего пола распределяется по всей поверхности примерно одинаково. Тогда остается излучение самих молекул воздуха. Молекулы имеют маленькую массу и охотно отзываются на собственный импульс придачи, после чего устремляются в том же направлении отстрела этого импульса. Статистически у теплых молекул частота излучения выше, чем у холодных. Они чаще отстреливают свои импульсы в пространство, где меньше давление, поэтому теплые молекулы летят в сторону потолка, освобождая место холодным. Получается, за счет этого электромагнитное, гравитационное излучение земли подтягивает к полу в большей степени холодный воздух, соответственно, теплый выталкивается вверх. Холодные молекулы имеют меньшую скорость, поэтому находятся в более плотном состоянии. Вот по такой технологии идет конвекция в любой газовой среде.
Теплый воздух в комнате выходит из температурного равновесия и постепенно внедряется в ряды холодного, отдавая часть своей теплоты.
3. Эйнштейн против Клапейрона и Менделеева
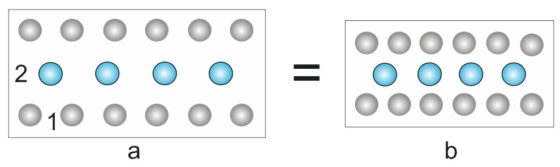
Рис. 2. На рисунке условно показано равное количество молекул азота (1) и молекул кислорода (2), находящихся при разных температуре и занимающих не равные объемы. a — при высокой температуре; b — при низкой температуре.
Обычно объясняют, что холодный воздух выталкивает теплый и тот поднимается вверх. На самом деле никто никого не толкает и не выталкивает. Весь воздух подвержен притяжению Земли и эта энергия его подпитывает. В зависимости от энергонасыщенности происходит температурная сегрегация по высоте расположения. Молекулы теплого воздуха имеют большую скорость перемещения, они разлетаются на большие расстояния, происходит больше столкновений между ними и они занимают больший объем (рис. 2а).
А теперь для доказательства равенства масс молекул, находящихся под разным тепловым потенциалом, я призвал на помощь два уравнения из классической физики.
1) уравнение состояния для идеального газа Клапейрона-Менделеева.
(1)
(2)
Где, m — масса газа, P — давление, V — объем, M — молярная масса, R — универсальная газовая постоянная, Т — температура.
Замечание, сейчас принято обозначать температуру греческой буквой Θ (Тэта). Чтобы не нарушать написание известной формулы оставим символ Т.
Из (2) видно, что при повышении температуры, увеличивается V (при постоянном давлении P). При этом масса газа (воздуха) остается постоянной.
2) Уравнение Эйнштейна. Энергия излучения связана с его массой.
E=mc2 (3)
m=E/c2 (4)
Подставив в формулы (3, 4) реальные значения, можно убедиться без лишних доказательств, что кубовый объем газа, имеющий меньшую энергию Е (температуру и скорость молекул) будет иметь и меньшую массу.
Тогда можно заключить, что холодный воздух легче теплого, и должен подниматься вверх, а он падает вниз. Вот где нелогичная конвекция и Эйнштейн против Клапейрона и Менделеева.
В чем же дело? А дело в серьезном разбирательстве, связанном со знаменитой формулой. Если в расчете использовать формулу (3), то килограммовый куб воздуха будет иметь энергию 9·1016 Дж. Данная величина приблизительно равна электрической энергии 3∙1010 кВт∙ч! Такое количество электроэнергии потребляют США за один день! Невероятно, но где энергия? А ее, увы, не видно.
Этому разбирательству посвящена отдельная статья под названием: «Энергия покоя». А сейчас, чтобы выбраться из создавшейся коллизии введем в данное уравнение энергетический коэффициент GE.
T — температура тела в Кельвинах
Tmax — максимально возможная температура вещества в природе.
E=GE·mc2 (5)
Отсюда масса
(6)
(7)
Используя в расчетах уравнение (7) можно убедиться, что при прочих равных условиях, массы холодного и теплого воздуха будут равны. Такой же расчет дает по формуле (2) Клапейрона-Менделеева и противостояние с Эйнштейном прекращается. И что самое главное, энергия газового куба снижается до удобоваримого значения, на десять порядков! Все расчеты привели меня к заключению, что уравнение Эйнштейна не общее, а частное, для максимального значения температуры при GE=1.
Электромагнитное, крафонное излучение Земли постоянно мониторит пространство и подтягивает атмосферу с паром вниз, но теплый воздух всегда оказываются наверху. Это происходит потому, что холодные молекулы реже отстреливают свои крафоны придачи в окружающее пространство из-за их меньшей энергонасыщенности.
Теплый воздух в комнате находится в термодинамическом равновесии, поэтому его молекулы продолжают хаотично двигаться, постепенно внедряясь в ряды холодного, отдавая часть своей теплоты.
Несмотря на то, что холодный воздух находится всегда внизу, масса теплых и холодных молекул остается одинаковой.
Конвективные перемещения в жидкости можно объяснить аналогичным способом.
Объемная плотность газа существенно зависит от температуры газа.
Как было указано выше, более горячий газ устремляется вверх не из-за его легкости, а по причине поднятия молекул за счет крафонного излучения. По сути, о какой легкости или тяжести мы говорим, каждая молекула находится во взвешенном состоянии, но не в какой-то среде, а фактически, в вакууме. Равные по массе и одинаковой температуре молекулы будут иметь одинаковый объемный вес. Известно, если охладить кубометр воздуха, то получим 1,2 литра в жидком состоянии. Отсюда вопрос: какое вещество занимает 998,8 литра этого объема воздуха, если мы уберем энергию расширения, то есть теплоту?!
- Перельман Я.И., Знаете ли вы физику? «ТЕРРА», М. 2007
Назад Вперед
Источник