Какие промежуточные продукты в цикле трикарбоновых кислот
Справочник химика 21
Глюкоза как субстрат. Важнейшими и наиболее распространенными анаплеротическими реакциями, восполняющими расход промежуточных продуктов цикла трикарбоновых кислот у животных, растений и микроорганизмов, являются реакции карбоксилирования Сз-кислот (пирувата, фосфоенолпирувата), ведущие к образованию оксалоацетата [c.248]
Если во время роста клеток промежуточные продукты цикла трикарбоновых кислот используются в биосинтетических процессах, недостаток этих продуктов компенсируется восполняющими (анаплеротическими) реакциями. Одна из функций таких реакций-регенерация оксалоацетата, из которого в результате взаимодействия с ацетилкоферментом А образуется цитрат. [c.248]
Глюконеогенез -синтез глюкозы из неуглеводных продуктов. Такими продуктами или метаболитами являются в первую очередь молочная и пировиноградная кислоты, так называемые гликогенные аминокислоты, глицерол и ряд других соединений. Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла трикарбоновых кислот . [c.338]
Чаще всего водород отнимается от промежуточных продуктов цикла трикарбоновых кислот (ЦТК) — цикла Кребса (изолимонная, а-кетоглутаровая, янтарная и яблочная кислоты). Цикл Кребса — это за- [c.136]
Промежуточные продукты цикла трикарбоновых кислот [44] [c.198]
Катаболизм промежуточных продуктов цикла трикарбоновых кислот [c.326]
В ЭТОЙ главе рассматривается биосинтез аминокислот и некоторых молекул, которые из них образуются. Прежде всего мы рассмотрим реакции, приводящие к включению азота в состав аминокислот. Этот путь начинается с восстановления N2 до в клетках азотфиксирующих микроорганизмов. Затем NH4 включается в аминокислоты через глутамат и глутамин, два ключевых соединения азотистого метаболизма. Десять из основного набора двадцати аминокислот синтезируются из промежуточных продуктов цикла трикарбоновых кислот и других метаболических последовательностей с помощью несложных реакций. Мы рассмотрим эти биосинтетические пути и опишем биосинтез ароматических аминокислот и гистидина в качестве примеров аминокислот, синтезирующихся более сложным образом. На самом деле человек должен получать эти десять аминокислот с пищей, потому их и называют незаменимыми аминокислотами. В этих реакциях участвуют два весьма любопытных посредника тетрагидрофолят, многоцелевой переносчик одноуглеродных единиц трех степеней окисления, и 5-аденозилметионин, главный донор метильных групп. Еще одна важная сфера наших интересов-регуляция метаболизма аминокислот. На примере глу-тамин-синтетазы мы проиллюстрируем некоторые общие принципы регуляции. Конец настоящей главы посвящен синтезу и распаду гема. [c.230]
Эффективность данного процесса, можно повысить, изучив-механизмы, регуляции метаболизма в микрофлоре систем с активным илом. Регуляция биодеградации- это. сложная задача. Однако, зная биохимию соответствующих процессов, мы,. по-виДимому, сможем вмешиваться, и в их регуляцию. Например, добавление к илу промежуточных продуктов цикла трикарбоновых кислот в низ 11х концентрациях (2-5 мг/л), глюкозы, аминокислот и витаминов (в частности, аланина и никотиновой кислоты) приводит к ускорению окисления ряда соединений. Введение этих промежуточных продуктов в состав, биомассы увеличивает энергетические потребности системы, стимулирует синтез АТР за счет усиленного окисления неорганических веществ типа серы или аммиака. Понимание биохимии подобных процессов, видимо, даст возможность вмешиваться в процессы регуляции метаболизма. [c.255]
Отсутствие любого из промежуточных продуктов цикла трикарбоновых кислот должно остановить дальнейшее функционирование цикла, если только другой продукт цикла не будет регенерироваться со скоростью, равной скорости исчезновения первого субстрата. Чаще [c.120]
Как происходит пополнение оксалоацетата Млекопитающие лишены ферментативного механизма, обеспечивающего превращение ацетил-СоА в оксалоацетат или другой промежуточный продукт цикла трикарбоновых кислот. Оксалоацетат у них образуется путем карбоксилирования пирувата, катализируемого пируват-карбоксилазой (разд. 15.15). [c.64]
Пермеазы — переносчики специфических метаболитов через биомембраны. Они напоминают ферменты, так как обладают специфичностью по отношению к определенным веществам, способны насыщаться при высоких концентрациях субстрата и могут подвергаться специфическому ингибированию. В митохондриях печени крыс были идентифицированы переносчики для АДФ, АТФ, фосфата, а также для некоторых промежуточных продуктов цикла трикарбоновых кислот. Наиболее хорошо изучен переносчик внутренней мембраны, осуществляющий перенос АДФ и АТФ — соединений, которые не могут проникать через мембрану путем диффузии. [c.121]
Анаплеротнческие реакции — ферментативные реакции, пополняющие запас промежуточных продуктов цикла трикарбоновых кислот, их еще называют возмещающими. Наиболее важная реакция такого рода — ферментативное карбокси-лирование пирувата с образованием оксалоацетата, катализируемая пируваткарбок-силазой. Когда цикл трикарбоновых кислот функционирует в условиях недостатка оксалоацетата или других промежуточных продуктов, реакция карбоксилирования пирувата стимулируется, в результате чего запас оксалоацетата растет. При избытке оксалоацетата может происходить декарбоксилирование с образованием пирувата [c.96]
Расщепление органических соединений в процессе дыхания также сопровождается субстратным фосфорилированием, но основное количество АТФ образуется при окислительном фосфорилировании, сопряженном с окислением промежуточных продуктов цикла трикарбоновых кислот. Общий выход АТФ на одну молекулу субстрата, окисленного при дыхании, значительно выше, чем при его сбраживании. [c.47]
Таким образом, пируват-карбоксилаза не только имеет важное значение для глюконеогенеза, но играет также критическую роль в поддержании необходимой концентрации промежуточных продуктов цикла трикарбоновых кислот. Указанные промежуточные продукты должны все время восполняться, поскольку они потребляются при некоторых биосинтетических реакциях, например при синтезе гема. Эта роль пируват-карбоксилазы получила название анаплеротической, что означает восполняющая, компенсирующая. [c.108]
Аминокислоты синтезируются из промежуточных продуктов цикла трикарбоновых кислот и других важных метаболитов [c.233]
Рассматривая различные стороны возможной корреляции между липогенезом и синтезом полиеновых антибиотиков, Т. Т. Ефимова и др. (1977) предполагают, что их образование лимитируется количеством пропионил-КоА, так как среди многочисленных жирных кислот у изученных продуцентов практически полностью отсутствовали жирные кислоты нормального строения с нечетным числом атомов углерода в цепи, синтез которых начинается с пропионил-КоА. Основным источником этого продукта является метилмалонил-КоА, который, в свою очередь, происходит из сукционил-КоА — промежуточного продукта цикла трикарбоновых кислот. Усиленному образованию пропионил-КоА способствует, по мнению -авторов, низкая активность сукционатдегидрогеназы, что для A t. levoris показали результаты исследований О. С. Кузнецовой (1975). Не исключается значение и других путей образования пропионил-КоА. [c.176]
Пируваткарбоксилаза-это митохондриальный фермент. Образовавшийся С-ок-салоацетат смешивается с пулом оксалоацетата, используемого в цикле трикарбоновых кислот. Следовательно, между С-оксалоацетатом и промежуточными продуктами цикла трикарбоновых кислот устанавливается равновесие с образованием через С-сукцинат смеси 1- С- и 4- С-оксалоацетата. Из оксалоацетата, меченного С в положении 1, образуется 3,4- С-глюкоза [см. задачу 2(6)]. [c.722]
Цикл трикарбоновых кислот не только выполняет функцию конечного окисления органических веществ, но и обеспечивает процессы биосинтеза различными предшественниками, такими как 2-оксоглутарат, оксалоацетат и сукцинат. Отсутствие этих кислот привело бы к нехватке оксалоацетата, который служит акцептором для ацетил-СоА, и тем самым к нарушению цикла. Восполнение потерь промежуточных продуктов цикла трикарбоновых кислот-функция так называемых анапле-ротических реакций. Важнейший механизм обеспечения цикла С4-дикарбоновыми кислотами состоит в карбоксилировании пирувата и фосфоенолпирувата (С3 + С — С ). Эти реакции будут подробнее рассмотрены позже (разд. 7.5). [c.234]
В качестве субстратов окисления (т. е. веществ, от которых отнимается водород) в тканевом дыхании используются разнообразные промежуточные продукты распада белков, углеводов и жиров. Однако наиболее часто окислению подвергаются промежуточные продукты цикла трикарбоновых кислот (ЦТК) — цикла Кребса (изолимонная, а-кетоглутароаая, янтарная и яблочная кислоты). Цикл Кребса — это за-верщающий этап катаболизма, в ходе которого происходит окисление [c.37]
До сих пор, обсуждая цикл трикарбоновых кислот, мы рассматриваем его как основной путь расщепления, обеспечивающий генерирование АТР. Однако цикл трикарбоновых кислот выполняет и другую роль он поставляет промежуточные продукты для процессов биосинтеза (рис. 13.15). Например, большинство углеродных атомов в порфи-ринах происходит из сукцинил-СоА, Многие аминокислоты происходят из а-оксоглута-рата и оксалоацетата. Биосинтез этих соединений мы рассмотрим в последующих главах. Здесь же необходимо отметить тот важный момент, что потребление промежуточных продуктов цикла трикарбоновых кислот для целей биосинтеза обязательно должно сопровождаться их пополнением. Предположим, например, что оксалоацетат превращается в аминокислоты, используемые для биосинтеза белка. Если при этом не будет происходить синтеза оксалоацетата de novo, то функционирование цикла трикарбоновых кислот прекратится, поскольку ацетил-СоА может включиться в цикл только после конденсации с оксалоацетатом. [c.64]
Активность пируват-карбоксилазы зависит от присутствия ацетил-СоА. В отсутствие связанного с ферментом аиетил-СоА (или другого близкого к нему ацил-СоА) биотин не карбоксилируется. Вторая частичная реакция не зависит от ацетил-СоА. Аллостерическая активация пируват-карбоксилазы при участии ацетил-СоА представляет собой важный физиологический механизм контроля. Оксалоацетат, продукт пируват-карбоксилазной реакции, является одновременно и стехиометрическим промежуточным продуктом глюконеогенеза, и каталитическим промежуточным продуктом цикла трикарбоновых кислот. Высокое содержание ацетил-СоА служит сигналом необходимости большего количества оксалоацетата. Если имеет место избыток АТР, оксалоацетат потребляется в процессе глюконеогенеза. В условиях недостатка АТР оксалоацетат включается в цикл трикарбоновых кислот, конденсируясь с аце-тил-СоА. [c.108]
Аспартат, аминокислота, содержащая четыре атома углерода, прямо трансаминирует-ся в оксалоацетат, промежуточный продукт цикла трикарбоновых кислот [c.168]
Глутамат синтезируется из NH4 и а-оксо-глутарата, промежуточного продукта цикла трикарбоновых кислот, под действием глутамат-дегидрогеназы. Мы уже встречались с этим ферментом в разделе, посвященном распаду аминокислот (разд. 18.1). Когда реакция идет в направлении биосинтеза, используется NADPH в качестве восстановителя когда же реакция является катаболиче-ской, в ней участвует NAD в качестве [c.232]
Биохимия Т.3 Изд.2 (1985) — [ c.64 , c.65 ]
Источник
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦИКЛ КРЕБСА)
Цикл трикарбоновых кислот впервые был открыт английским биохимиком Г. Кребсом. Он первым постулировал значение данного цикла для полного сгорания пирувата, главным источником которого является гликолитическое превращение углеводов. В дальнейшем было показано, что цикл трикарбо-новых кислот является тем центром, в котором сходятся практически все метаболические пути. Таким образом, цикл Кребса — общий конечный путь окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе катаболизма большая часть органических молекул, играющих роль «клеточного топлива»: углеводов, жирных кислот и аминокислот.
Образовавшийся в результате окислительного декарбоксилирования пирувата в митохондриях ацетил-КоА вступает в цикл Кребса. Данный цикл происходит в матриксе митохондрий и состоит из восьми последовательных реакций (рис. 10.9). Начинается цикл с присоединения ацетил-КоА к оксалоацетату и образования лимонной кислоты (цитрата). Затем лимонная кислота (шестиуглеродное соединение) путем ряда дегидрирований (отнятие водорода) и двух декарбоксилирований (отщепление СО2) теряет два углеродных атома и снова в цикле Кребса превращается в оксалоацетат (четырехуглеродное соединение), т.е. в результате полного оборота цикла одна молекула ацетил-КоА сгорает до СО2 и Н2О, а молекула окса-лоацетата регенерируется. Рассмотрим все восемь последовательных реакций (этапов) цикла Кребса.
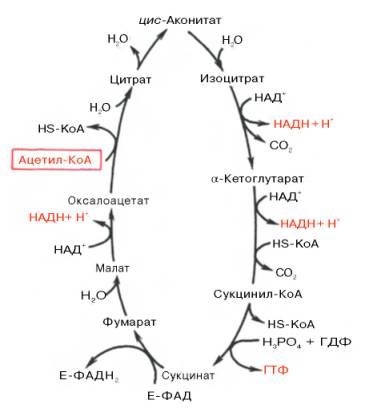
Рис. 10.9. Цикл трикарбоновых кислот (цикл Кребса).
Первая реакция катализируется ферментом цит-рат-синтазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота:
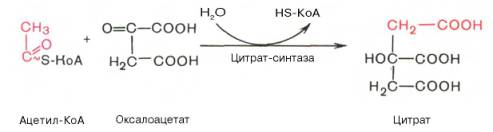
По-видимому, в данной реакции в качестве промежуточного продукта образуется связанный с ферментом цитрил-КоА. Затем последний самопроизвольно и необратимо гидролизуется с образованием цитрата и HS-KoA.
В результате второй реакции образовавшаяся лимонная кислота подвергается дегидратированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат). Катализирует эти обратимые реакции гидратации-дегидратации фермент аконитатгидратаза (аконитаза). В результате происходит взаимоперемещение Н и ОН в молекуле цитрата:
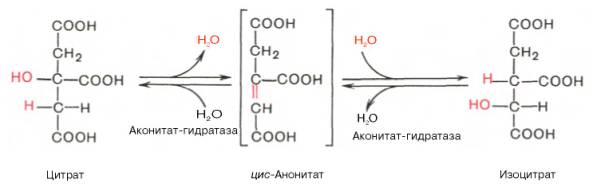
Третья реакция, по-видимому, лимитирует скорость цикла Кребса. Изолимонная кислота дегидрируется в присутствии НАД-зависимой изо-цитратдегидрогеназы.
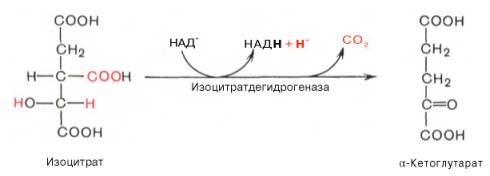
В ходе изоцитратдегидрогеназной реакции изолимонная кислота одновременно декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg2+или Мn2+.
Во время четвертой реакции происходит окислительное декарбокси-лирование α-кетоглутаровой кислоты с образованием высокоэнергетического соединения сукцинил-КоА. Механизм этой реакции сходен с таковым реакции окислительного декарбоксилирования пирувата до ацетил-КоА, α-кетоглутаратдегидрогеназный комплекс напоминает по своей структуре пируватдегидрогеназный комплекс. Как в одном, так и в другом случае в реакции принимают участие 5 коферментов: ТПФ, амид липоевой кислоты, HS-KoA, ФАД и НАД+.
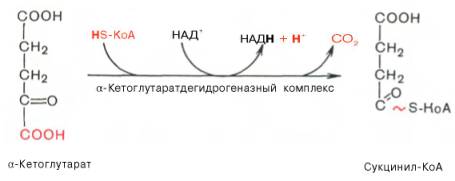
Пятая реакция катализируется ферментом сукцинил-КоА-синтета-зой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической фосфатной связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА:
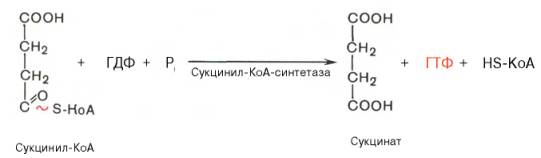
В результате шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком прочно (ковалентно) связан кофермент ФАД. В свою очередь сукцинатдегидрогеназа прочно связана с внутренней ми-тохондриальной мембраной:
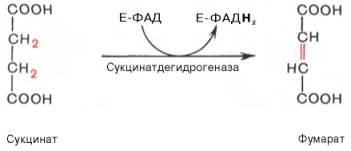
Седьмая реакция осуществляется под влиянием фермента фума-ратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является яблочная кислота (малат). Следует отметить, что фумаратгидратаза обладает стереоспецифичностью (см. главу 4) — в ходе реакции образуется L-яблочная кислота:
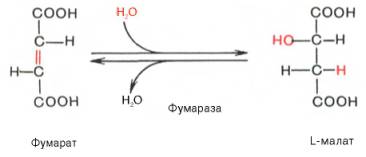
Наконец, в ходе восьмой реакции цикла трикарбоновых кислот под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат:

Как видно, за один оборот цикла, состоящего из восьми ферментативных реакций, происходит полное окисление («сгорание») одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД+ и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. Это окисление осуществляется в системе переносчиков электронов в дыхательной цепи (в цепи дыхательных ферментов), локализованной в мембране митохондрий. Образовавшийся ФАДН2 прочно связан с СДГ, поэтому он передает атомы водорода через KoQ. Освобождающаяся в результате окисления ацетил-КоА энергия в значительной мере сосредоточивается в макроэргических фосфатных связях АТФ. Из 4 пар атомов водорода 3 пары переносят НАДН на систему транспорта электронов; при этом в расчете на каждую пару в системе биологического окисления образуется 3 молекулы АТФ (в процессе сопряженного окислительного фосфорилирования), а всего, следовательно, 9 молекул АТФ (см. главу 9). Одна пара атомов от сукцинатдегидрогеназы-ФАДН2 попадает в систему транспорта электронов через KoQ, в результате образуется только 2 молекулы АТФ. В ходе цикла Кребса синтезируется также одна молекула ГТФ (субстратное фосфорилирование), что равносильно одной молекуле АТФ. Итак, при окислении одной молекулы ацетил-КоА в цикле Кребса и системе окислительного фосфорилирования может образоваться 12 молекул АТФ.
Если подсчитать полный энергетический эффект гликолитического расщепления глюкозы и последующего окисления двух образовавшихся молекул пирувата до СО2 и Н2О, то он окажется значительно большим.
Как отмечалось, одна молекула НАДН (3 молекулы АТФ) образуется при окислительном декарбоксилировании пирувата в ацетил-КоА. При расщеплении одной молекулы глюкозы образуется 2 молекулы пирувата, а при окислении их до 2 молекул ацетил-КоА и последующих 2 оборотов цикла трикарбоновых кислот синтезируется 30 молекул АТФ (следовательно, окисление молекулы пирувата до СО2 и Н2О дает 15 молекул АТФ). К этому количеству надо добавить 2 молекулы АТФ, образующиеся при аэробном гликолизе, и 6 молекул АТФ, синтезирующихся за счет окисления 2 молекул внемитохондриального НАДН, которые образуются при окислении 2 молекул глицеральдегид-3-фосфата в дегидрогеназной реакции гликолиза. Следовательно, при расщеплении в тканях одной молекулы глюкозы по уравнению С6Н12О6 + 6О2 -> 6СО2 + 6Н2О синтезируется 38 молекул АТФ. Несомненно, что в энергетическом отношении полное расщепление глюкозы является более эффективным процессом, чем анаэробный гликолиз.
Необходимо отметить, что образовавшиеся в процессе превращения глицеральдегид-3-фосфата 2 молекулы НАДН в дальнейшем при окислении могут давать не 6 молекул АТФ, а только 4. Дело в том, что сами молекулы внемитохондриального НАДН не способны проникать через мембрану внутрь митохондрий. Однако отдаваемые ими электроны могут включаться в митохондриальную цепь биологического окисления с помощью так называемого глицеролфосфатного челночного механизма (рис. 10.10). Ци-топлазматический НАДН сначала реагирует с цитоплазматическим ди-гидроксиацетонфосфатом, образуя глицерол-3-фосфат. Реакция катализи-
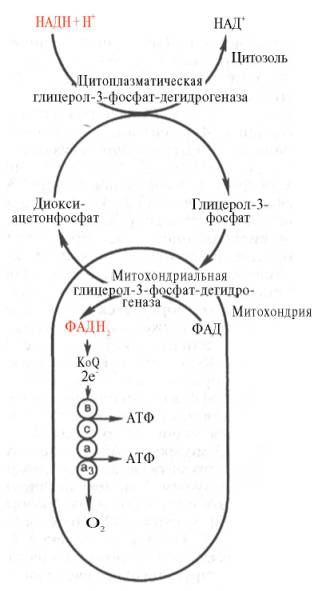
Рис. 10.10. Глицеролфосфатный челночный механизм. Объяснение в тексте.
руется НАД-зависимой цитоплазматической глицерол-3-фосфат-дегидроге-назой:
Дигидроксиацетонфосфат + НАДН + Н+ <=> Глицерол-3-фосфат + НАД+.
Образовавшийся глицерол-3-фосфат легко проникает через митохонд-риальную мембрану. Внутри митохондрии другая (митохондриальная) глицерол-3-фосфат-дегидрогеназа (флавиновый фермент) снова окисляет глицерол-3-фосфат до диоксиацетонфосфата:
Глицерол-3-фосфат + ФАД <=> Диоксиацетонфосфат + ФАДН2.
Восстановленный флавопротеин (фермент-ФАДН2) вводит на уровне KoQ приобретенные им электроны в цепь биологического окисления и сопряженного с ним окислительного фосфорилирования, а диоксиаце-тонфосфат выходит из митохондрий в цитоплазму и может вновь взаимодействовать с цитоплазматическим НАДН + Н+. Таким образом, пара электронов (из одной молекулы цитоплазматического НАДН + Н+), вводимая в дыхательную цепь с помощью глицеролфосфатного челночного механизма, дает не 3, а 2 АТФ.
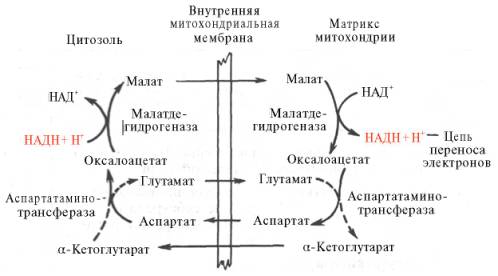
Рис. 10.11. Малат-аспартатная челночная система для переноса восстанавливающих эквивалентов от цитозольного НАДН в митохондриальный матрикс. Объяснение в тексте.
В дальнейшем было показано, что с помощью данного челночного механизма лишь в скелетных мышцах и мозге осуществляется перенос восстановленных эквивалентов от цитозольного НАДН + Н+ в митохондрии.
В клетках печени, почек и сердца действует более сложная малат-ас-партатная челночная система. Действие такого челночного механизма становится возможным благодаря присутствию малатдегидрогеназы и ас-партатаминотрансферазы как в цитозоле, так и в митохондриях.
Установлено, что от цитозольного НАДН + Н+ восстановленные эквиваленты сначала при участии фермента малатдегидрогеназы (рис. 10.11) переносятся на цитозольный оксалоацетат. В результате образуется малат, который с помощью системы, транспортирующей дикарбоновые кислоты, проходит через внутреннюю мембрану митохондрии в матрикс. Здесь малат окисляется в оксалоацетат, а матриксный НАД+ восстанавливается в НАДН + Н+, который может теперь передавать свои электроны в цепь дыхательных ферментов, локализованную на внутренней мембране митохондрии. В свою очередь образовавшийся оксалоацетат в присутствии глутамата и фермента АсАТ вступает в реакцию трансаминирования. Образующиеся аспарат и α-кетоглутарат с помощью специальных транспортных систем способны проходить через мембрану митохондрий.
Транспортирование в цитозоле регенерирует оксалоацетат, что вызывает к действию следующий цикл. В целом процесс включает легкообратимые реакции, происходит без потребления энергии, «движущей силой» его является постоянное восстановление НАД+ в цитозоле гли-церальдегид-3-фосфатом, образующимся при катаболизме глюкозы.
Итак, если функционирует малат-аспартатный механизм, то в результате полного окисления одной молекулы глюкозы может образоваться не 36, а 38 молекул АТФ (табл. 10.1).
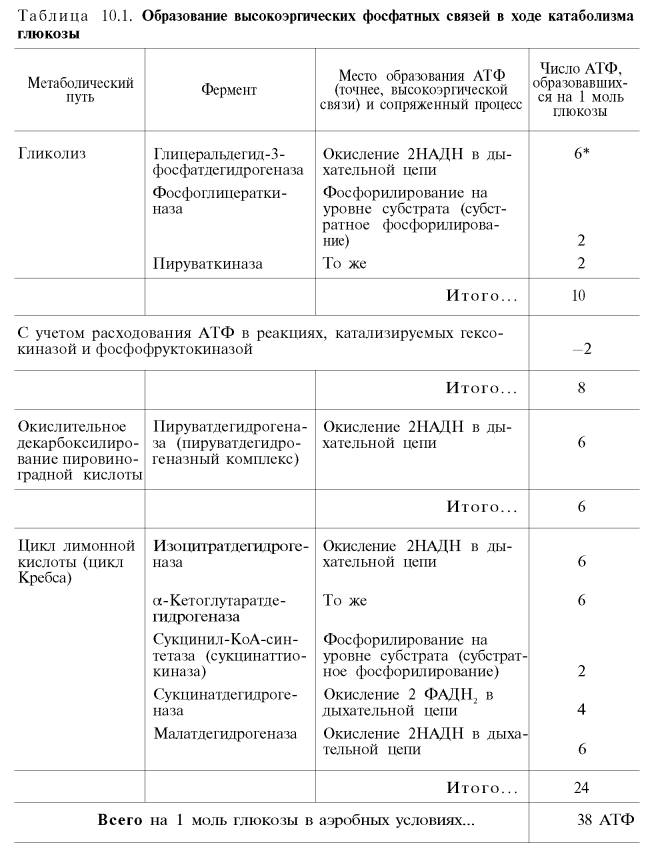
В табл. 10.1 приведены реакции, в которых происходит образование высокоэргических фосфатных связей в ходе катаболизма глюкозы, с указанием эффективности процесса в аэробных и анаэробных условиях.
Еще по теме:
- ТРИКАРБОНОВЫХ КИСЛОТ ЦИКЛ — химическая энциклопедия
- трикарбоновых кислот цикл — химическая энциклопедия
Источник